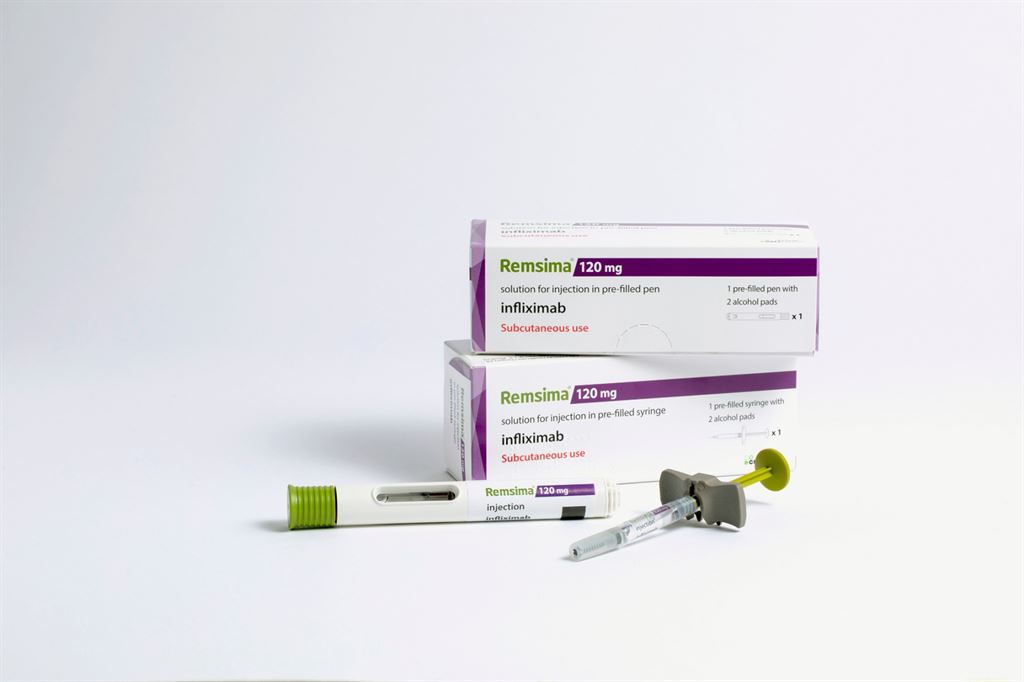
[포쓰저널=김지훈 기자] 셀트리온은 세계 최초 인플릭시맙 피하주사 제제 '램시마SC'가 25일 유럽의약품청(EMA) '판매 승인’을 획득했다고 26일 밝혔다.
램시마SC는 램시마를 기존 정맥주사(IV)에서 피하주사(SC)로 제형을 변경해 자체 개발한 바이오의약품이다.
EMA에서는 심사 과정부터 바이오베터(biobetter)로서, 확장 신청이라는 기존 바이오시밀러와 차별화된 승인 절차를 밟아 왔다.
바이오베터는 오리지널 바이오의약품을 기반으로 효능이나 안전성, 편의성 등을 개량한 약을 말한다.
지난 9월 EMA 산하 약물사용자문위원회(CHMP)는 램시마SC '판매 승인 권고' 의견을 공표한 바 있다.
이번 판매 승인 획득으로 셀트리온은 130여 개국에 램시마SC의 특허출원을 완료할 예정이다.
셀트리온 관계자는 “셀트리온은 이미 세계 유수의 학회를 통해 램시마SC 임상 결과를 발표하며 안전성과 효능을 입증했으며 이를 바탕으로 램시마SC의 시장 진입에 대해 유럽 의료진들의 큰 기대를 확인할 수 있었다”면서 “셀트리온헬스케어는 램시마SC의 시판을 계기로 유럽 시장에서 다른 바이오시밀러와 차별화된 프라임급 위치에서 시장점유율을 확대할 계획이다. 램시마SC가 매출 증대와 수익성 개선에도 큰 몫을 할 것”이라고 말했다.
김지훈 기자
4th.hun@gmail.com