18세 이상 접종 2주뒤 66.9% 예방효과
국내 허가 백신 AZ, 화이자 이어 세번째
정부 600만명 분 계약.."상반기 도입 추진"
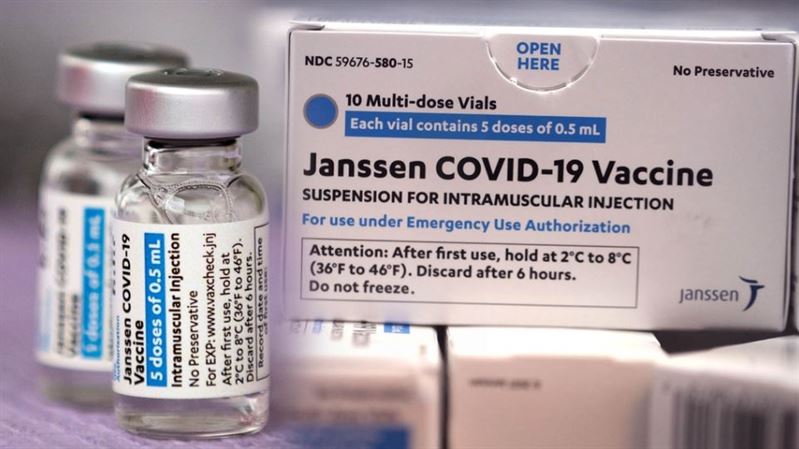
[포쓰저널=조혜승기자] 미국 얀센(존슨앤존슨 자회사)의 코로나19 백신이 7일 식품의약품안전처로부터 최종 품목허가를 받았다.
얀센 백신은 아스트라제네카, 화이자에 이어 국내 의료당국의 허가를 받은 세 번째 코로나19 백신이다. 여타 백신과 달리 1회 접종만으로 예방효과를 볼 수 있어 '게임 체인저'로 주목받고 있다.
식약처는 이날 외부 전문가가 포함된 최종점검위원회를 열고 얀센의 코로나19 백신 ‘코비드-19백신 얀센주’에 대한 품목허가를 결정했다고 밝혔다.
단 허가 후 임상시험 최종결과보고서를 제출하는 조건이다.
식약처는 얀센 백신 예방효과에 대해 만 18세 이상 1회 투여 14일 후 66.9%, 28일 후 66.1%의 예방 효과를 보여 효과성을 인정할 수 있다고 판단했다.
안전성에서는 크게 이상이 없었다. 보고된 이상사례의 대부분이 주사부위 통증, 두통, 피료, 근육통 등 ‘매우 흔하게’ 나타나는 증상이었으며, 대부분 증상이 경증에서 중간 정도 수준으로 백신 접종 후 2~3일 이내 회복됐다고 식약처 측은 설명했다. '매우 흔하게'라는 기준은 10%이상 나타나는 이상사례를 말한다.
구체적으로 보면 임상시험 등록 대상자 4만3783명 중 백신군 0.4%(83명), 대조군 0.4%(96명)에서 이상사례가 보고됐다. 이 가운데 '중대한 이상반응'은 상완신경근염 등 7건이었으나 임상시험 자료 제출 시점에는 대부분 회복중인 점을 고려해 식약처 측은 문제가 없다고 봤다.
식약처는 미국과 벨기에 1·2상에서 수행된 임상시험 1건, 일본 1상 1건, 독일 등 다국가 2상 1건, 미국 등 8개국 3상에서 수행된 임상시험 1건 등 총 4건을 검토했다.
안전성과 효과성은 미국 등에서 수행된 임상 3상을 통해 평가했다.
최종점검위원회의 결정에 따라 얀센 백신은 검증 자문단, 중앙약심에 이어 백신 검증 3중 자문 절차를 모두 통과했다.
코비드-19백신 얀센주는 미국 다국적제약사 존슨앤드존슨의 제약부문인 얀센이 개발한 바이러스 벡터 방식의 백신이다.
코로나 바이러스 표면항원 유전자를 재조합해 사람 아데노바이러스에 넣어 체내에 주입해 항원단백질을 합성한다. 이 단백질이 중화항체의 생성을 유도해 바이러스를 중화해 제거하는 방식이다.
앞서 국내 허가를 받은 아스트라제네카, 화이자 백신과 달리 한 번만 맞아도 되는 장점이 있다. 보관 조건은 –25~15도에서 24개월이다.
얀센 백신은 유럽, 미국, 스위스 등 35개 국가와 세계보건기구(WHO)에서 조건부 허가 또는 긴급사용승인을 받은 상태다.
정부는 얀센과 백신 600만명분에 대한 구매 계약을 체결했다.
정세균 국무총리는 2일 올해 상반기 내 1200만명 이상 접종이 이뤄질 수 있도록 얀센, 노바백스, 모더나 등 백신에 대해 조기도입을 추진하겠다고 밝힌 바 있다.
얀센 백신의 구체적인 도입 일정은 미정이다.
김강립 식약처장은 “이 제품이 허가된 이후에도 질병청 등과 협력해 접종 후 이상 사례에 대해 감시체계를 강화하고 철저한 모니터링과 대응을 통해 국민들께서 안심하고 접종받으실 수 있도록 최선을 다하겠다”고 말했다.